每日經濟新聞 2022-03-17 12:10:22
◎3月16日,君實生物又披露了一份關于VV116公布3項I期臨床數據的公告。研究結果顯示,VV116在健康受試者中表現出令人滿意的安全性和耐受性,且口服吸收迅速,可在空腹或普通飲食條件下口服用藥,建議在后續臨床研究中探索每日兩次200毫克至600毫克給藥劑量。
每經記者 許立波 每經編輯 魏官紅
君實生物(688180.SH)連續發布了兩份關于其口服抗新冠病毒藥物VV116的臨床試驗進展公告。
3月15日晚間,君實生物公告稱,由公司控股子公司君拓生物與旺山旺水合作開發的口服核苷類抗SARS-CoV-2藥物VV116片(以下簡稱VV116)已啟動了一項三期臨床研究,并完成了首例患者的入組及給藥。該三期臨床研究旨在評估VV116用于中重度新型冠狀病毒肺炎受試者治療時,對比標準治療的有效性和安全性,是一項國際多中心的隨機、雙盲、對照研究。
3月16日,君實生物又披露了一份關于VV116公布3項I期臨床數據的公告。公告顯示,藥學領域知名期刊Acta Pharmaceutica Sinica發表了口服核苷類抗SARS-CoV-2藥物VV116的3項I期臨床研究結果。研究結果顯示,VV116在健康受試者中表現出令人滿意的安全性和耐受性,且口服吸收迅速,可在空腹或普通飲食條件下口服用藥,建議在后續臨床研究中探索每日兩次200毫克至600毫克給藥劑量。這是國產口服小分子抗SARS-CoV-2藥物首次公布I期臨床數據。
根據一份君實生物方面提供給《每日經濟新聞》記者的材料,VV116此次發表的3項I期臨床研究均由上海市徐匯區中心醫院劉罡一主任、余琛主任擔任主要研究者。其中研究1(NCT05227768)和研究2(NCT05201690)為隨機、雙盲、安慰劑對照、單劑量和多劑量遞增研究,旨在評估在健康受試者中單次和多次遞增口服VV116的安全性、耐受性和藥代動力學特征;研究3(NCT05221138)是一項隨機、開放、3周期、交叉研究,旨在觀察飲食對健康受試者口服VV116后藥代動力學和安全性的影響。
研究在2021年11月至2022年1月間,共納入86名符合標準的成年健康受試者,研究1納入38名受試者,研究2納入36名受試者,研究3納入12名受試者。
研究結果顯示:
(1)VV116口服吸收迅速。在單次遞增劑量研究中,口服VV116后可迅速水解為活性代謝產物116-N1,平均血漿藥物達到峰值時間(Tmax)僅為1.00小時-2.50小時。此外,116-N1的平均半衰期(t 1/2)值為4.80小時-6.95小時,提示在臨床治療中可探索每日兩次(BID)的給藥方案。
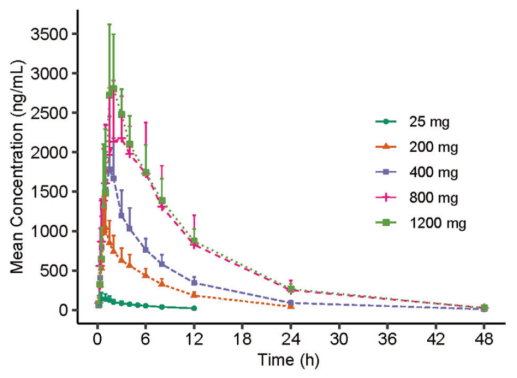
圖1:單次給藥后各劑量組血漿中116-N1的平均濃度-時間曲線
(2)重復給藥可維持有效抗病毒濃度。在多次遞增劑量研究中,連續每日兩次給藥(間隔12小時),持續5.5天(第1天至第6天),3個劑量組(200mg、400mg和600mg)體內藥物濃度均可維持在有效的抗病毒水平之上(谷濃度大于抗奧密克戎變異株的EC90)。

圖2:多次遞增劑量研究中第1天和第6天血漿中116-N1的平均濃度-時間曲線
(3)普通飲食對VV116藥物暴露量無影響。空腹、普通飲食和高脂飲食條件下的中位Tmax分別為1.50小時、3.00小時和2.50小時,表明飲食會延長藥物達到峰值的時間,但并不影響藥物的峰濃度。高脂飲食略增加了血藥濃度一時間曲線下面積(AUC),建議可在空腹或在普通飲食條件下進行藥物口服治療。
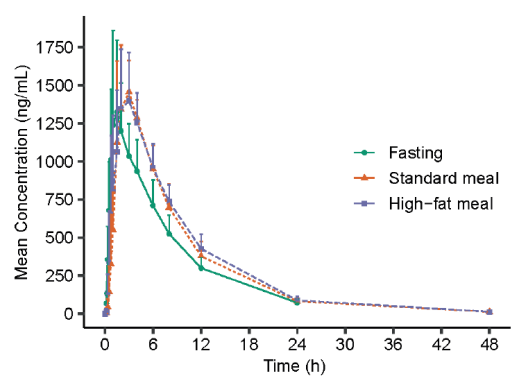
圖3:空腹和進食條件下血漿中116-N1的平均濃度-時間曲線
在安全性方面,VV116在健康受試者中顯示出令人滿意的安全性及耐受性。3項研究均未報告死亡、未發生嚴重不良事件(SAE)、未發生3級及以上不良事件(AE),也未出現導致停藥及中斷治療的AE。所有AE均在未治療或未干預情況下恢復。相較同類藥物在過往報告的數據,VV116具有較低的肝毒性風險。
基于VV116 I期研究的積極結果,君實生物與旺山旺水已啟動一項國際多中心、雙盲、隨機、安慰劑對照、II/III期臨床研究(NCT05242042),針對輕中度COVID-19患者。該研究由復旦大學附屬華山醫院張文宏教授和上海市公共衛生臨床中心沈銀忠教授聯合主持,旨在評價VV116用于輕中度COVID-19患者早期治療的有效性、安全性和藥代動力學。此外,另一項在中重度COVID-19患者中評價VV116有效性和安全性的國際多中心、隨機、雙盲、對照III期臨床研究正在進行中。
封面圖片來源:攝圖網-500327248
如需轉載請與《每日經濟新聞》報社聯系。
未經《每日經濟新聞》報社授權,嚴禁轉載或鏡像,違者必究。
讀者熱線:4008890008
特別提醒:如果我們使用了您的圖片,請作者與本站聯系索取稿酬。如您不希望作品出現在本站,可聯系我們要求撤下您的作品。
歡迎關注每日經濟新聞APP
