每日經濟新聞 2021-08-19 18:09:18
◎索元生物的7個在研藥品來源皆為外采,包括禮來、奧爾巴尼、百時美施貴寶、強生等。實際上,索元生物在從事一個“撿漏”的事情,就是挑別家藥企已經宣告失敗的項目再進行操作,而其中核心關鍵點就在于能否找到“生物標志物”。
◎索元生物的核心產品,也是募投金額最多的產品是DB102。對于該產品,索元生物稱已經發現了生物標志物。“截至本招股說明書簽署日,公司核心產品DB102對應的2項研究正處于III期臨床試驗階段,距離提交新藥上市申請仍需一段時間,在此過程中可能會面臨藥品注冊審評制度的變動”。
每經記者 趙李南 每經實習記者 林姿辰 每經編輯 陳俊杰
杭州索元生物醫藥股份有限公司(以下簡稱索元生物)近期遞交了招股書(申報稿,下同),擬在科創板IPO,募集資金16億元。
《每日經濟新聞》記者注意到,索元生物頗有一些特殊之處,按照公司說法,其是一家以高效的精準醫療技術開發多款面向全球市場的首創新藥(First-in-class)的生物醫藥公司。而索元生物的特殊性就體現在其所有的研發管線皆是靠外采,而其中不乏有長達6年的外采研發項目尚未取得實質研發進展的情況。
此外,截至2020年底,索元生物總計有員工數43人,其中境內員工數12人。
2018年度至2020年度,索元生物實現營業收入分別為0、10.35萬元和10.35萬元;實現歸屬于母公司所有者的凈利潤分別約為-1億元、-1.34億元和-2.23億元。
索元生物表示:“發行人處于新藥研發階段,核心產品尚未取得上市許可,未發生與其核心產品相關的銷售。報告期內,發行人的收入均為DB102商業化開發許可的期權費收入。”
索元生物所提及的DB102是其研發管線中的一個,公司以編號的方式命名研發管線,除此之外還有DB103、DB104、DB105、 DB106、DB107、DB108。
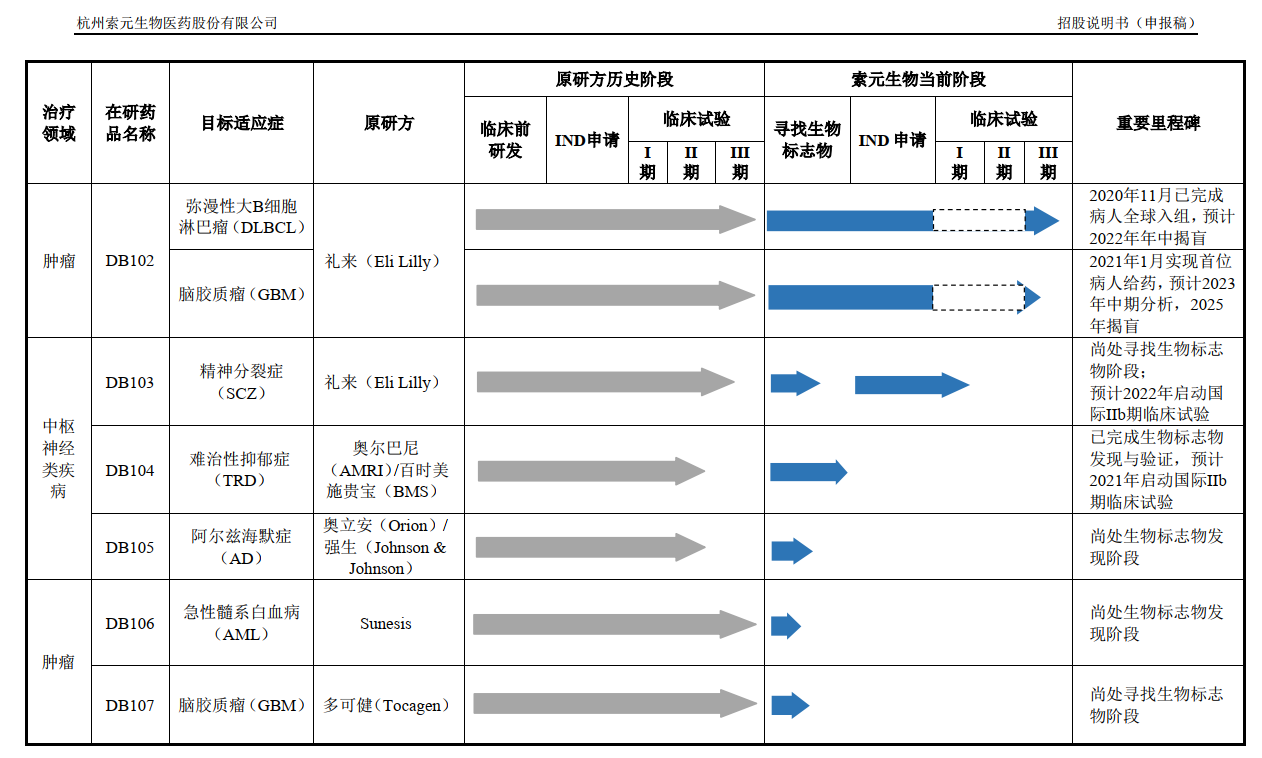
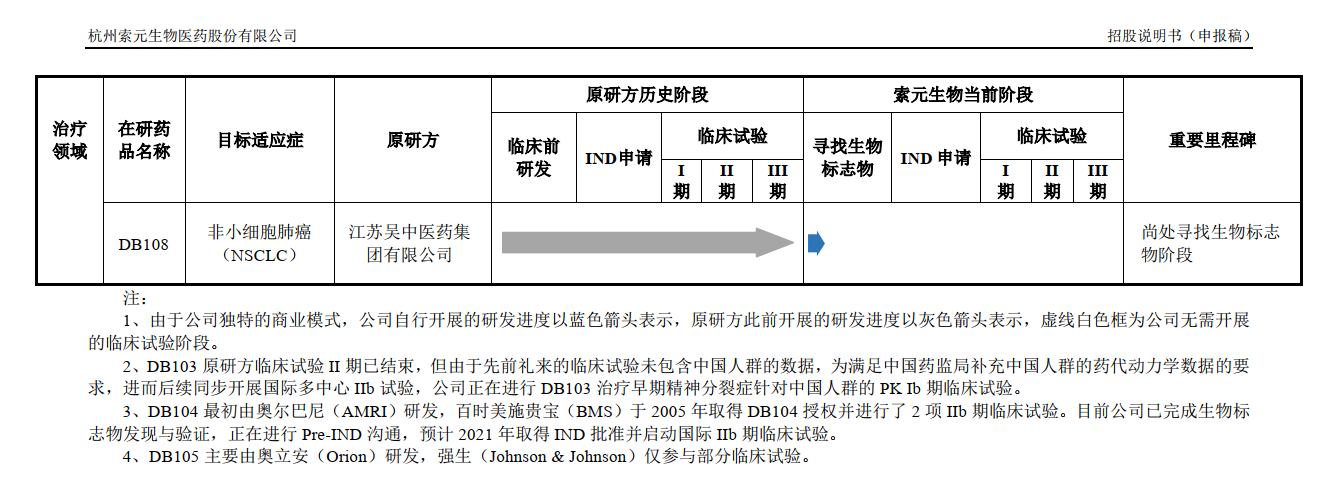
圖片來源:索元生物招股書截圖
值得注意的是,索元生物的7個在研藥品來源皆為外采,包括禮來、奧爾巴尼、百時美施貴寶、強生等。
對于為何沒有自主研發的藥品,索元生物表示:“公司針對未滿足臨床需求的重大疑難病癥,如腫瘤及中樞神經類疾病,收購或引進后期臨床試驗失敗但已證明其安全性且顯示對部分患者有效的創新藥,并獲得該等創新藥的全球或全球絕大部分地區權益。通過公司獨特的生物標志物發現平臺,尋獲到經獨立驗證的可預測藥效的生物標志物,進而重新開展以生物標志物為指導的國際多中心臨床試驗,最終開發出面向全球市場的創新藥。”
換句話說,索元生物在從事一個“撿漏”的事情,就是挑別家藥企已經宣告失敗的項目再進行操作,而其中核心關鍵點就在于能否找到“生物標志物”。
在前述的研發藥品中,DB102、DB103和DB104是索元生物的募投項目,擬募集投入的資金分別約為6億元、2.7億元和7億元。
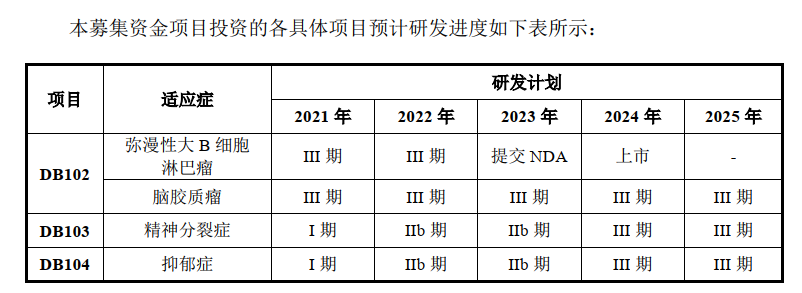
圖片來源:索元生物招股書截圖
《每日經濟新聞》記者了解到,DB103的化合物名稱為Pomaglumetad Methionil,是禮來原研的抗精神分裂藥物,臨床III 期試驗未達預期效果。
索元生物針對該藥的研究還停留在“尋找生物標志物階段”,“目前DB103正處于尋找生物標志物階段。公司已完成DB103 相關樣本的全基因組掃描,正在進行全基因組掃描結果分析”。
事實上,早在2012年8月,禮來就已經宣布停止對pomaglumetad methionil的研發。而索元生物雖然沒有在招股書中披露對DB103的引入時間,但卻在其美國子公司官網上的新聞稿中披露了該藥物的引入時間為2015年3月。
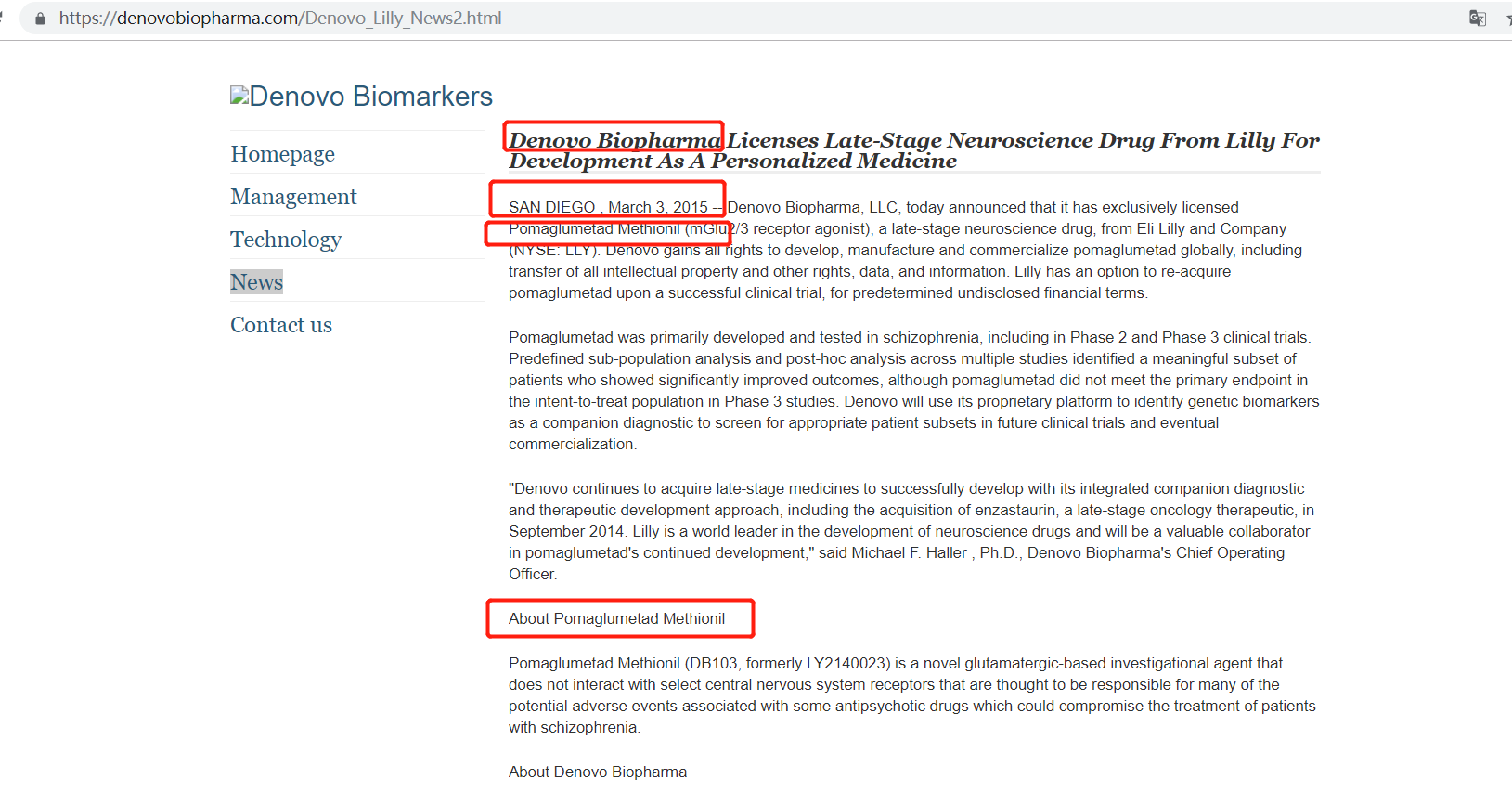
圖片來源:索元美國官網截圖
在上述新聞稿中,索元生物表示:“Pomaglumetad主要在精神分裂癥中開發和測試,包括在2期和3期臨床試驗中。多項研究中的預定義亞群分析和事后分析確定了一個有意義的患者子集,這些患者顯示出顯著改善的結果,盡管pomaglumetad在3期研究中未達到意向治療人群的主要終點。索元生物將使用其專有平臺來識別遺傳生物標志物作為伴隨診斷,以在未來的臨床試驗和最終商業化中篩選合適的患者亞群。”
換句話說,在2015年3月,索元生物取得DB103的許可之時,便已經要進行“生物標志物”的識別研究,而迄今為止,這個識別已經跨越了6年還未有成果。
相比之下,索元生物已經宣稱發現的DB102的生物標志物DGM1,DB104的生物標志物DGM4所花費的時間都未超過4年。
針對DB103的研究進展問題,索元生物方面向《每日經濟新聞》記者表示:“公司于2015年收購DB103,目前DB103正處于尋找生物標志物階段。公司發現潛在生物標志物的階段,是一個極為復雜的原創科學發現的過程,需要依賴藥學、臨床醫學、分子生物學、生物信息學、基因組學、遺傳學和統計學等各方面專家的緊密合作,需要極強的專業知識和技術訣竅(即Know-how)。此外,中樞神經系統疾病發病機制尤為復雜、臨床效果較難評測,均增加了中樞神經系統疾病相關藥物的生物標志物發現的難度。相對于腫瘤領域精準醫療的突飛猛進,目前在中樞神經疾病創新藥研發領域,全球范圍內尚未有可預測藥效藥物基因組生物標志物的獲批上市,還未實現零的突破。盡管公司運用其生物標志物開發平臺為腫瘤新藥成功發現生物標志物,DB103是公司第一次嘗試將該平臺用于中樞神經疾病。”
此外,索元生物還表示:“自公司完成DB103全球授權及技術轉移以來,公司運用了多種組學手段進行了全基因掃描,并開發了多種針對中樞神經類疾病的新的算法來進行大規模數據分析。正是受益于進行DB103項目時開發出的新算法及對中樞神經類疾病臨床試驗終點的了解,公司通過其獨特的生物標志物發現平臺,于2019年發現了一個全新的與中樞神經系統領域另外一款藥物DB104降低抑郁癥主要臨床指標MADRS評分的高度相關的生物標志物,命名為DGM4(Denovo Genomic Marker 4)。”
索元生物的核心產品,也是募投金額最多的產品是DB102。對于該產品,索元生物稱已經發現了生物標志物。
“截至本招股說明書簽署日,公司核心產品DB102對應的2項研究正處于III期臨床試驗階段,距離提交新藥上市申請仍需一段時間,在此過程中可能會面臨藥品注冊審評制度的變動。”索元生物表示。
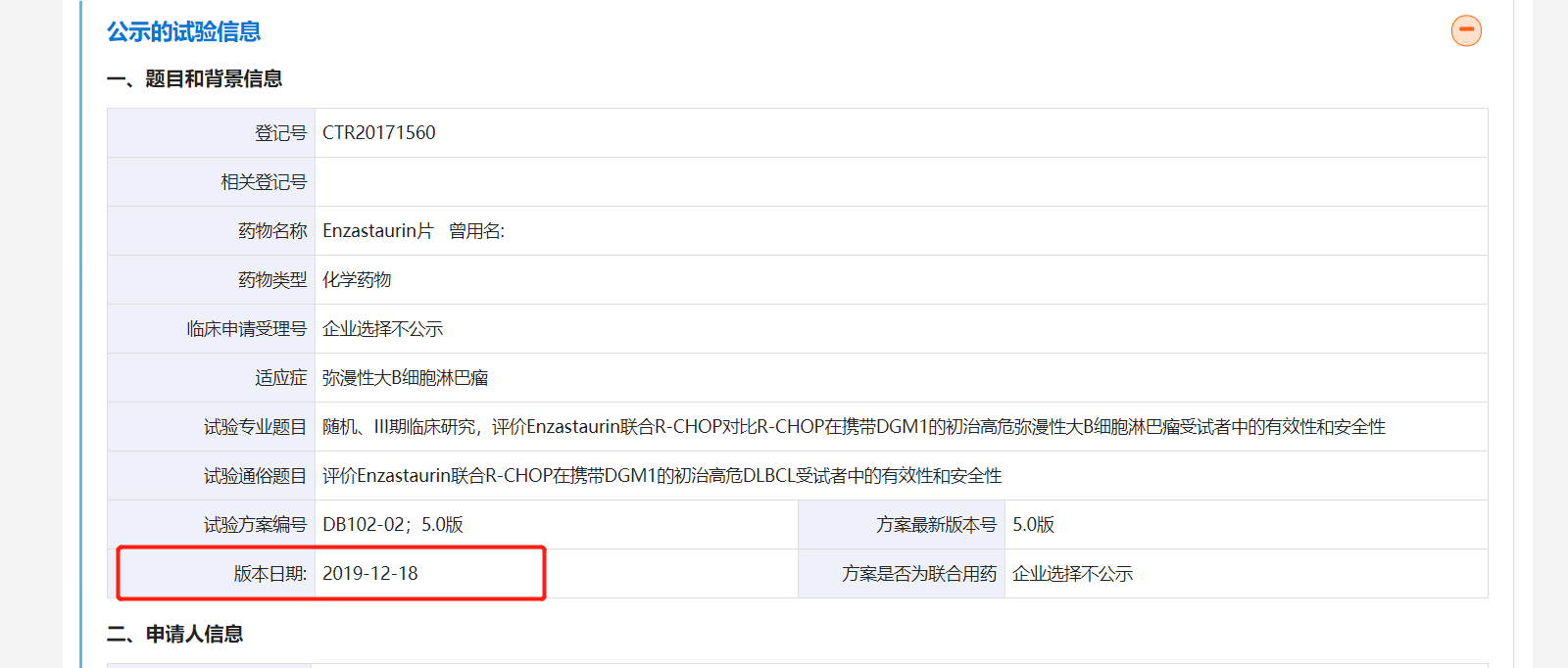
在招股書中,索元生物對該藥品III期臨床試驗的進度相應表述為:“DB102 正在中國和美國同步開展國際多中心,一線治療彌漫性大B細胞淋巴瘤(DLBCL)III期臨床試驗研究,已于2020年11月完成國際多中心臨床III期病人入組,預計將于2022年年中揭盲。”
事實上,索元生物僅在招股書中描述了DB102的III 期臨床試驗完成入組時間,但并未公布該III期臨床試驗的開始時間。《每日經濟新聞》記者發現,在藥物臨床試驗登記與信息公示平臺公示的信息顯示,DB102的III期臨床試驗早在2018年3月就已經開始,迄今為止已經有3年半的時間。
值得注意的是,編號為CTR20171560的DB102 III期臨床試驗在2019年12月18日版本的公示信息中,已經顯示“招募完成”,目標入組人數為國內120人,國際235人;已入組人數為國內176人,國際256人。
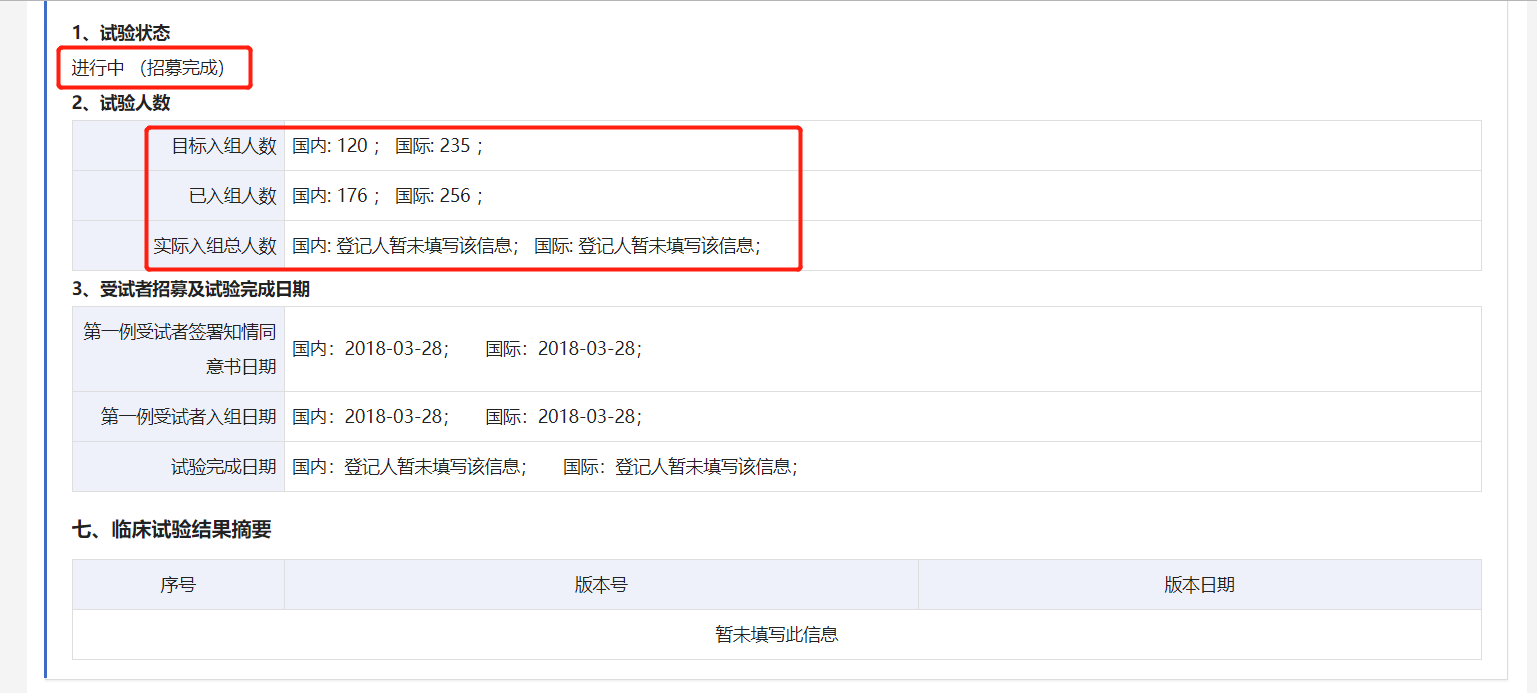
圖片來源:藥物臨床試驗登記與信息公示平臺截圖
為何該三期試驗已經持續了相當長的時間還未有結果?《每日經濟新聞》記者向索元生物發送了采訪函。
索元生物回復稱:“DB102正在中國和美國同步開展國際多中心一線治療彌漫性大B細胞淋巴瘤(DLBCL)III期臨床試驗研究,主要療效終點是DGM1生物標志物陽性受試者的OS(OS是指從隨機分組日期至任何原因死亡日期之間這段時間)。在腫瘤領域,有OS、PFS、TPP、TFF、ORR、DCR、DDC等各項評價指標。其中OS被認為是腫瘤臨床試驗中最具有臨床價值的療效終點,所以它是本試驗的首要臨床終點。但是采用OS會導致臨床試驗持續時間較長。相比于其他惡性腫瘤,DLBCL中位OS相對較長,如果以OS為臨床主要終點,臨床試驗通常需要較長時間,例如跟本實驗較為類似的禮來的一線治療DLBCL的臨床II期臨床試驗用了近5年時間。”
索元生物表示:“該研究于2018年初展開,已于2020年11月完成國際多中心臨床III期病人入組,目前該試驗的揭盲時間受到終點事件(受試者死亡)發生的速度等各種因素的影響,預計將于2022 年年中揭盲,從全球多中心III期臨床試驗展開到揭盲預計耗時4年多。”
8月6日,該試驗的中國總協調研究者,北京腫瘤醫院教授朱軍向記者表示:“這個實驗我們還沒有揭盲,剛剛完成入組,正在收集數據整理待批,所以說這個實驗算是入組結束,但是數據的整理還沒完。原計劃5年,基本按計劃(進行),對這個試驗有信心。”
封面圖片來源:攝圖網
如需轉載請與《每日經濟新聞》報社聯系。
未經《每日經濟新聞》報社授權,嚴禁轉載或鏡像,違者必究。
讀者熱線:4008890008
特別提醒:如果我們使用了您的圖片,請作者與本站聯系索取稿酬。如您不希望作品出現在本站,可聯系我們要求撤下您的作品。
歡迎關注每日經濟新聞APP
