每日經濟新聞 2020-09-28 08:38:33
每經記者 金喆 每經編輯 文多

■公司:康方生物-B(09926,HK)
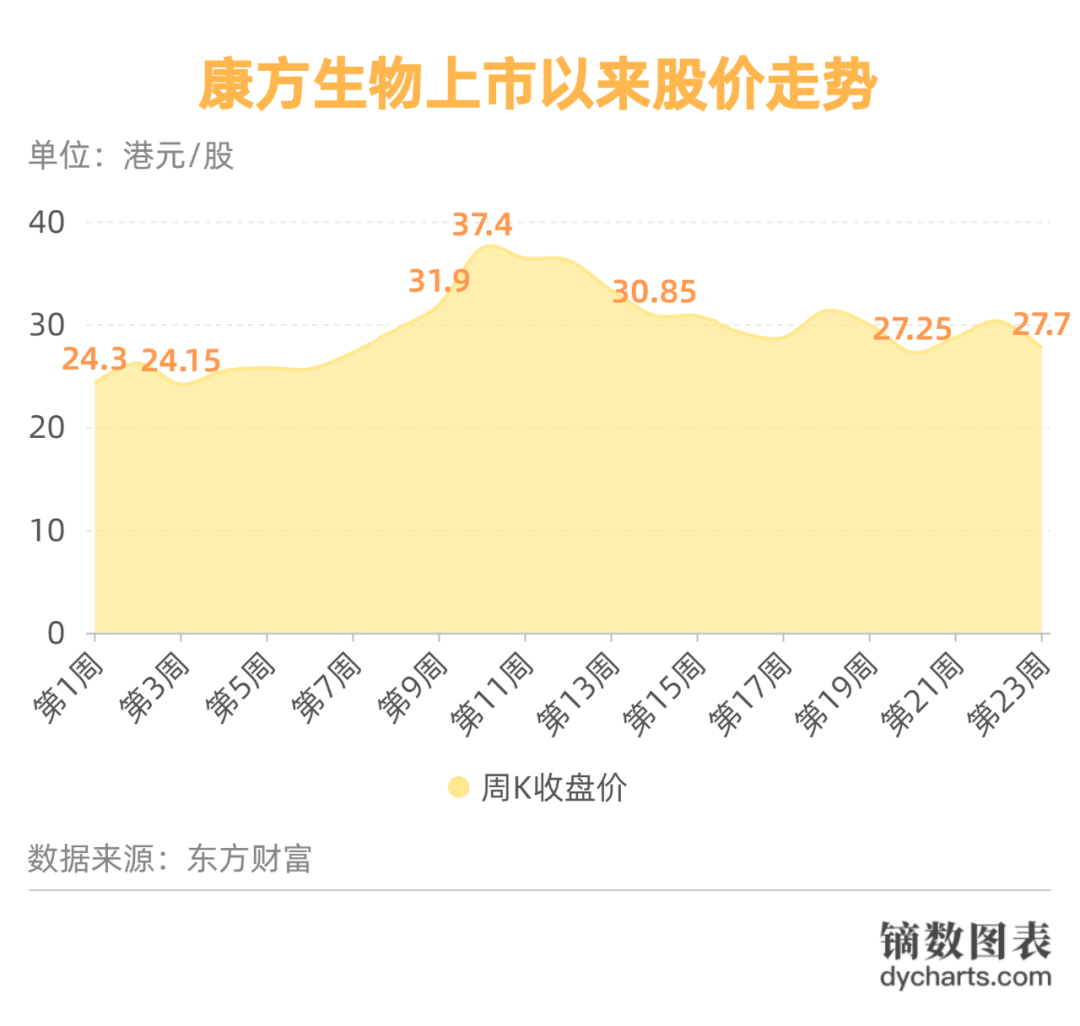
■市值:218.01億港元(截至9月25日)
■核心競爭力:豐富多樣的抗體藥物管線;開創性地向默沙東授權使用公司自主研發的CTLA-4抗體藥物;潛在下一代全球首創PD-1/CTLA-4雙抗;與中國生物制藥合作開發及商業化PD-1單抗
■機構眼中的公司:實力強勁的一體化創新型生物制藥公司、研發即將進入收獲期、商業化布局已進入日程
若干年后,站在中國制藥創新的歷史長河中回首,或許今天會是一個劃時代的節點。
中國制藥產業一直在期待自己的基因泰克(Genentech,全球著名生物科技企業),幸運的是,過去10年中終于看到了希望。自2010年開始,百濟神州、信達生物、君實生物、康方生物等本土新一代創新型生物醫藥企業相繼誕生,時至今日,他們已經成為中國醫藥創新的領頭羊。
在中國醫藥產業深度轉型的當下,這批創新企業自帶“時代主角光環”。而康方生物聯合創始人、董事長兼首席執行官夏瑜博士,正是中國新一代創新企業的創始人代表之一。2012年,夏瑜與3位朋友兼伙伴一起,在廣東省中山市創辦了康方生物,夏瑜回顧說,這里遠離熱鬧的長三角,適合潛心做科研。
“康方至今沒有考慮過做任何生物類似藥,我們所有在研管線都是新分子。”夏瑜近日接受《每日經濟新聞》記者專訪時,再次明確康方生物的發展戰略。
如今,康方生物經過8年征途,在今年4月登陸港交所,頂著“中國制藥新勢力”的光環,康方生物將在何時上市第一款藥,未來如何在中國甚至全球創新藥的舞臺走得更遠?這些,都是夏瑜從創業以來就一直在思考的問題。

截至今年6月30日,康方生物9種臨床階段抗體候選藥物開發狀況。
圖片來源:公司2020半年報截圖(點擊圖片可放大)

只做"first-in-class"的中國制藥新勢力

在創辦康方生物之前,夏瑜在歐美等全球創新前沿陣地沉淀了21年:從留學英國紐卡斯爾大學,到在英國格拉斯哥大學等從事研究工作,再到于德國拜耳等全球頂尖藥企負責各類研發和企業管理工作。也是這段履歷,讓她從外部深刻認識到了中國醫藥創新和國際領先水平的差距。
2007年夏瑜回國時,中國生物制藥正在經歷從無到有的階段,一批先知先覺的藥企嗅到轉型信號,開始研發“me-too”(模仿創新藥)類藥物,稍微改變原研藥的化學結構后進行仿制。這是創新藥研發的初級階段,稍微高級的,則是“me-better”(跟進創新藥)。
在生物制藥領域擁有20多年從業經驗的夏瑜認為,生物科技公司的使命是做創新型產品。但在2012年之前,中國的新藥研發可謂一片空白。所以,她和康方生物其他3位創始人的想法很簡單,就是想成立一家做新藥研發的中國公司,而且只做"first-in-class"(首創新藥),實實在在做出能在國際上比拼、處于國際領先的產品。
為什么是必須是創新藥?
夏瑜認為,開發成功一種真正具有創新性的新藥,對于創新性企業來說是最有價值的,也是公司社會價值和商業價值最直接的體現。那時,團隊的理想自然而然就實現了。對于創新,康方生物創始團隊為自己設立的目標也很長遠——在全球生物醫藥行業的創新領域做一顆常青樹,能夠久遠地占有一席之地。
接受《每經人物·專訪董事長》欄目專訪時,夏瑜也向記者提到了她對仿制藥的看法。她認為,生物類似藥在開發過程中避免了很多風險,時間投入也會少一些,這樣生產出來一種和原研藥一樣的藥物,本身對老百姓而言絕對是好事。但她也說道,從企業經營發展的長遠性來說,生物類似藥的門檻相對于首創藥物低了很多,競爭會很激烈。
經過8年創業,憑借著豐富的在研管線和快速推進的研發進度,康方生物被業內貼上“中國制藥新勢力”的標簽,并在國際舞臺嶄露頭角。
“在我看來,酒香不怕巷子深,很多事情(經過)一步一步努力,后來是水到渠成的事情。2015年以前的‘默默無聞’(時期),是我們潛心于研發創新的重要階段,就有點像我們四個人的標簽和理念,注重的是實實在在的事情。”夏瑜記得,過去8年(2012~2020年)里,很多時候研發團隊都在默默無聞地埋頭做事,雖然會遇到一些坎坷,但都會一起想辦法解決,從沒有想過放棄。
康方生物也確實做到了在行業內快人一步。在很多企業做生物類似藥的時候,康方早一步建立了完善的抗體藥物開發平臺,啟動新藥研發;在大家開始布局原創藥物的當下,康方生物已經建立了有著超20個在研管線的強大在研梯隊,對全球主要布局的抗體靶點均實現了布局。
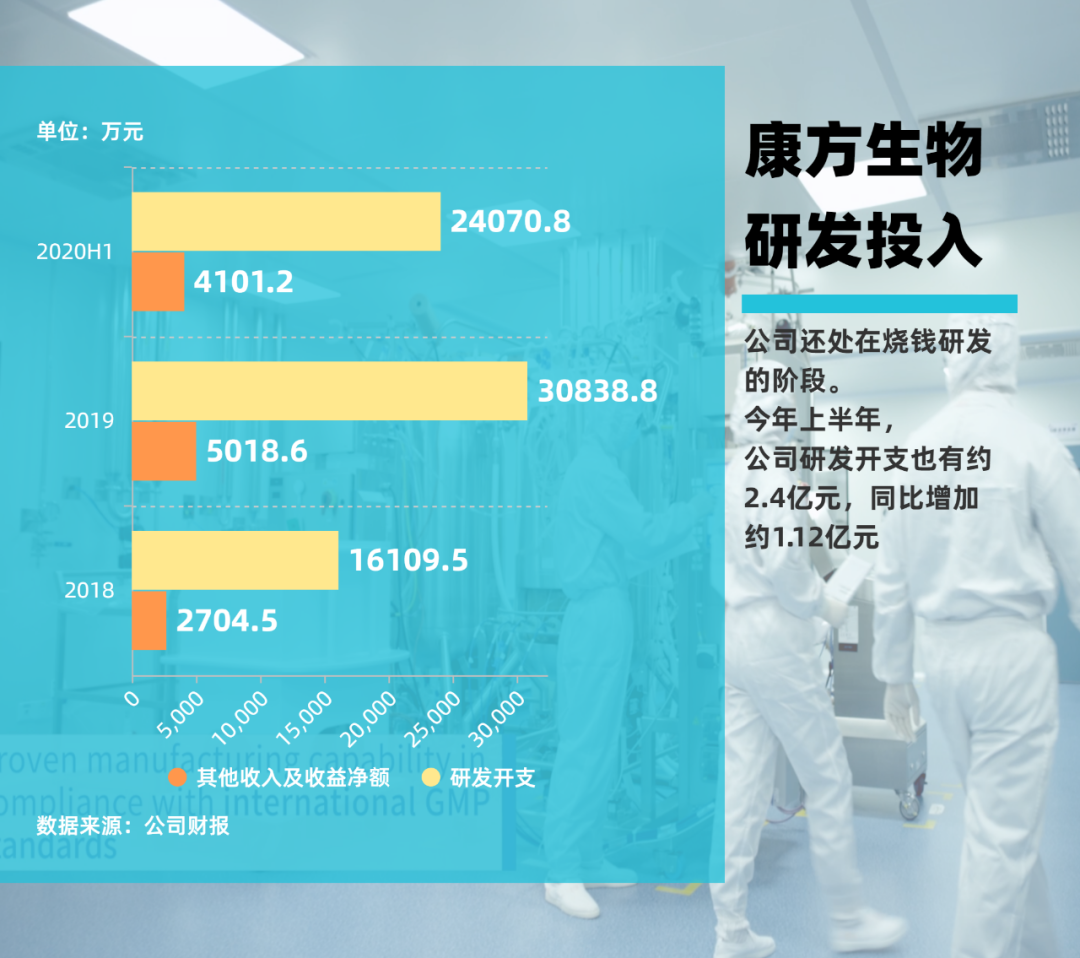
作為一家創新藥企業,康方生物還處在燒錢研發的階段。半年報顯示,公司今年上半年虧損6.73億元,其中研發開支約2.4億元,同比增加約1.12億元。其所有重點推進的候選藥物全部進入臨床階段,目前進入臨床的產品已經達到12個。

中國創新藥正被認可:讓世界感覺到欣喜和希望

對于夏瑜來說,過去的8年是康方生物的創業期,也是中國創新藥從無到有、從跟隨仿制到被世界認可的成長史。
這8年,對比強烈。夏瑜還記得,2008年她在中美冠科擔任副總裁時,哪怕在中國,CRO公司的客戶里都沒有中國本土企業;創立康方后,她才了解到當時國內的新藥審評審批速度。對當年的這些不利局面,她甚至笑言:“如果一開始知道這個情況的話,我可能不會創業。”
開弓沒有回頭路,雖然創新藥研發環境與發達國家存在差距,夏瑜與團隊還是要推進項目。
2014年,夏瑜與當時任職默沙東的化學家孫勇奎在一場活動上約了一起吃頓三明治午餐,進行了大約30分鐘的匆忙交流。借助這次交流,夏瑜希望對方能夠初步了解康方,并到中山實地參觀考察。
半年后,孫勇奎應邀前往。這次出行,為后來康方生物在創新藥領域一炮而紅埋下伏筆。2015年底,康方生物將用于腫瘤免疫治療的免疫檢查點阻斷CTLA-4抗體的全球獨家開發、推廣權,授予默沙東,該抗體正是在中國研發的。
授權跨國巨頭研發和推廣中國公司研發的產品,這在當時還是比較罕見的事情。在康方生物與默沙東合作以前,比較類似的事件,還是2013年11月,另一制藥巨頭默克雪蘭諾,獲得了百濟神州在研藥物BGB-290(PARP抑制劑)在中國以外市場的開發權。
如今,越來越多這樣的中國創新藥研發的企業被跨國醫藥巨頭看到,并展開合作。
2018年以后,君實生物、信達生物、百濟神州、復宏漢霖各自開發的PD-1藥物,也開始在國內市場與跨國藥企“掰手腕”。

圖片來源:受訪方提供
最近,夏瑜也收到一個令她備受鼓舞的好消息:康方生物在研的雙抗產品AK104,獲得了美國食品藥品監督管理局(FDA)快速審批資格。
AK104是新一代的抗腫瘤免疫治療藥物,是康方生物利用其獨特的Tetrabody雙抗技術,自主研發的首款雙抗產品。截至目前,全球僅批準了3個雙抗藥物,其中兩款與腫瘤適應癥相關的產品都涉及CD3靶點,而AK104是全球首個進入臨床試驗的PD-1/CTLA-4雙特異抗體。
AK104獲得FDA快速審批資格,這讓夏瑜感到非常欣喜——這意味著在未來AK104整個注射性臨床的發展過程中,他們都能與監管方有很好的交流,并且獲得排在優先級的審批流程。
“至少目前我們反饋給FDA的結果,讓他們感覺到欣喜和希望,認為是在這個領域有一些突破性的東西。”夏瑜覺得,就康方生物新藥研發來講,這是一個很重要的里程碑,公司最具創新性的產品獲得了國際級的認可,在全球化道路上邁出了堅實的一步。
夏瑜還指出,就競爭和策略來說,康方生物雙抗藥物的靶點布局和研發進展在國際上已屬領先——布局了6個全新靶點的雙抗產品,其中2個進入了臨床。
隨著雙抗產品的上市、成熟,下一階段雙抗藥物將會成為公司的基石產品,然后以其為基礎,開發更新一代的抗腫瘤藥物。

圖片來源:受訪方提供

超40臨床試驗在推 基石產品PD-1或明年上市

業界通常以“Biotech”和“BioPharma”來界定創新藥企業的兩種不同商業模式。
Biotech,即生物科技公司,以創新藥物的研發為核心業務,往往在新藥開發到二期、三期臨床時,把藥物出售給大型制藥企業,或是將公司出售,一般不涉及產品上市后的生產與銷售環節。
BioPharma,指生物制藥企業,它們從研發階段成長起來,業務覆蓋研發、產品銷售等各個環節。
對于康方生物這樣一家尚無產品上市的創新藥企而言,任何一款在研藥物的研發進展都意味著離上市更近一步。因此,何時迎來第一款上市產品也是外界特別關注的問題。
夏瑜欣喜地告訴《每日經濟新聞》記者,目前共有超過40個臨床試驗在推進。這在當前——特別是在新冠疫情期間,是一件非常高效的事情。從結果導向看,上半年的臨床開發,也確實取得了幾個比較重要的里程碑式進展。
首先,前文提到的AK104獲得了很好的進展,其不僅于近日通過FDA快速審批的資格認證,還在中國進行宮頸癌注冊性臨床試驗。
其次,在成熟產品方面,第一款自研創新藥PD-1抗體藥物派安普利單抗(AK105),在今年5月向國家藥監局新藥申報了上市申請,其適應癥為經典型霍奇金淋巴瘤(cHL),這也為商業化邁出了很重要的一步。
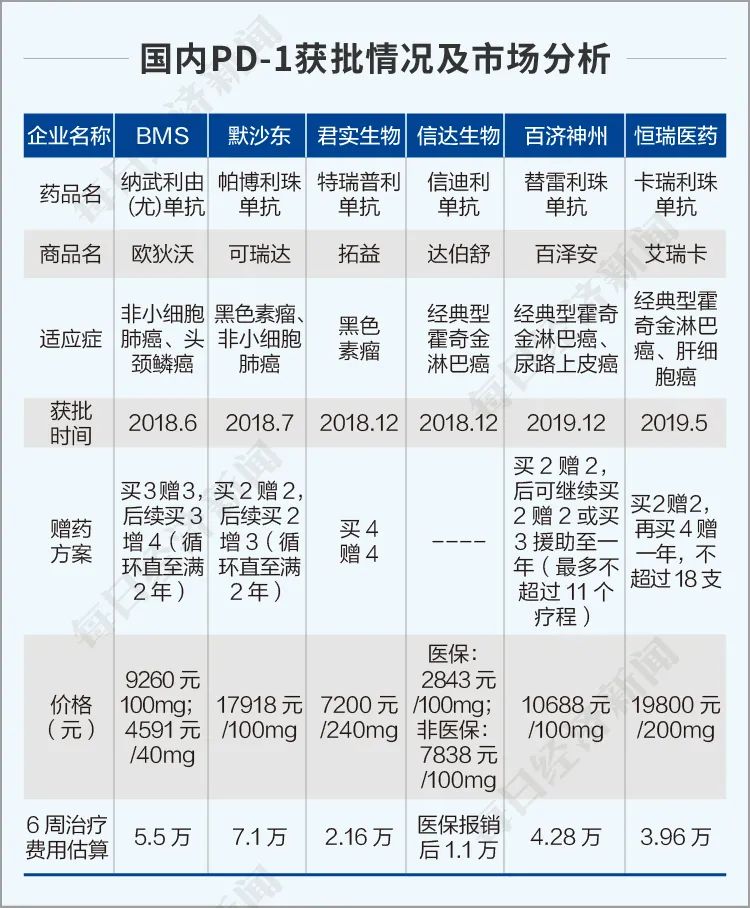
但一個不容忽視的現狀是,當前國內PD-1領域競爭白熱化,已經有6款產品獲批上市,適應癥的研究競爭也格外激烈。
目前,康方生物沒有在PD-1單藥(此處單藥是相對于聯合用藥而言)賽道上搶得上市先機,接下來打算如何實現彎道超車?
對此,夏瑜表示:PD-1是當前腫瘤領域的基石品種,而雙特異性抗體是康方生物的護城河,團隊在不放棄開發PD-1單藥的同時,也正努力做出優于PD-1的新一代產品。
《每日經濟新聞》記者注意到,為了加速PD-1產品上市,康方生物在去年6月與正大天晴成立合資公司,共同開發并推動該藥物的注冊上市及商業化。在夏瑜表示,這個時間節點,康方生物需要聯合正大天晴這樣銷售實力強大的公司布局PD-1的未來銷售。在下一階段,雙抗藥物有可能就會成為康方生物的基石產品。
在PD-1的競爭策略上,康方生物聯合正大天晴實現“超車”的重點,落在了產品創新和聯合療法帶來的臨床效果提升。一方面,據夏瑜介紹,康方生物在兩個生物學功能上做了修飾,力求比市場上的PD-1藥物有更好的有效性和安全性,正大天晴的銷售能力也是合作的優勢之一。另外,PD-1藥物的適應癥覆蓋面非常廣、市場非常巨大,還可能和一些抗癌藥聯合用藥,達到更高效、更好的治療效果。
可以看出,最近半年康方生物在整體布局上取得了很多進展,夏瑜透露,未來一兩年是重要的收獲期。
從戰略的角度來講,公司希望首先推進PD-1藥物在明年上市。
之后,在雙特異性抗體打出品牌、在國際上能占一席之位后,再有條不紊地開發創新靶點和非腫瘤的藥。
接下來,在明年后某個時間點,PD-1藥物之外的產品會進入商業化階段。對這一步,公司現在已經開始進行商業化的積極布局,不管是銷售還是生產方面,都已經啟動布局。

圖片來源:受訪方提供
夏瑜也把PD-1看做康方生物新發展周期的一個起點。她指出,經過8年多努力,康方生物已經建立了在全球范圍內都非常有競爭力的在研管線,根據全球市場的競爭態勢和自身優勢,通過戰略選擇性地推進產品研發,市場競爭能力上會逐步體現出系統性。考慮到公司目前20多個在研管線的推進以及部分重點產品陸續進入上市籌備階段,從布局上來講,目前的人員遠遠不夠,未來一兩年研發團隊、臨床團隊、銷售團隊和生產團隊人員都會有很大增加。
無論是對于康方生物,還是對中國創新藥行業來說,已知靶點終究會做完,未來國內新藥研發成功率會降低。站在中國制藥黃金十年的新起點,在中國做出好藥、讓中國制藥工業在世界領先,是全行業期待的美好愿景。

記者手記|Biotech企業是中國創新藥的新活力
評判一家Biotech企業是否年輕且有張力,從企業的戰略就能看出來。
同樣是把錢都投去做研發,有的布局風險更高的前沿,有的選擇相對穩妥的跟隨;同樣是選擇對外合作,有些是用自己的產品吸引跨國合作伙伴,有些是從海外合作伙伴手上尋求好品種。夏瑜帶領的康方生物,正是從成立初就選擇了前沿路線,就像她說的,康方不會做生物類似藥,只做best-in-class。
記者電話采訪夏瑜當天,康方生物AK104剛剛獲得美國FDA快速審批資格。這是對康方的認可,也是對中國藥企創新實力的認可。當越來越多像康方生物這樣的Biotech企業獲得國際認可,我們就有信心喊出:中國的醫藥研發實力正在走強,醫藥大國變醫藥強國的夢想終會實現。
記者:金喆
編輯:文多
視覺:劉陽
排版:文多 陳彥希
如需轉載請與《每日經濟新聞》報社聯系。
未經《每日經濟新聞》報社授權,嚴禁轉載或鏡像,違者必究。
讀者熱線:4008890008
特別提醒:如果我們使用了您的圖片,請作者與本站聯系索取稿酬。如您不希望作品出現在本站,可聯系我們要求撤下您的作品。
歡迎關注每日經濟新聞APP
